(通讯员:李梦玲 王爽爽)近日,五楼自拍
动物科学技术学院、动物医学院陶攀教授团队在Nature Communications发表题为 “Periplasmic gatekeeping of phage DNA entry by an rSAM enzyme matured effector with HxS repeats” 的研究论文。该研究发现了一种新型细菌抗噬菌体防御系统HXS,揭示了细菌可通过自由基S-腺苷甲硫氨酸酶(rSAM)介导效应蛋白成熟加工,并在细菌周质间隙抑制噬菌体DNA注入宿主的新机制。
噬菌体是能感染并裂解细菌的天然病毒,被认为是应对细菌耐药性危机的重要工具。然而,细菌在长期进化过程中形成了复杂多样的抗噬菌体防御系统,是开发高效噬菌体产品、防控耐药菌的主要障碍。已报道的细菌防御系统主要在噬菌体DNA进入细胞后,通过降解噬菌体核酸或诱导感染中止等方式发挥抗噬菌体作用。相比之下,针对噬菌体基因组DNA注入过程的细菌内源性防御机制此前尚不清楚。
本研究在大肠杆菌中鉴定出一种具有广谱抗噬菌体活性的新型防御系统HXS,在测试的113株噬菌体中可防御110株。该系统由HxsA、HxsB、HxsC和HxsD四个蛋白组成,其中HxsB和HxsC属于rSAM 酶家族,HxsA 含有5个高度保守的His-Xaa-Ser(HxS)重复结构。机制研究表明,HxsB、HxsC 和HxsD协同参与HxsA的成熟加工,包括N端切割以及特定位点的共价修饰。成熟后的HxsA被转运至细菌周质空间,抑制噬菌体基因组进入宿主细胞。
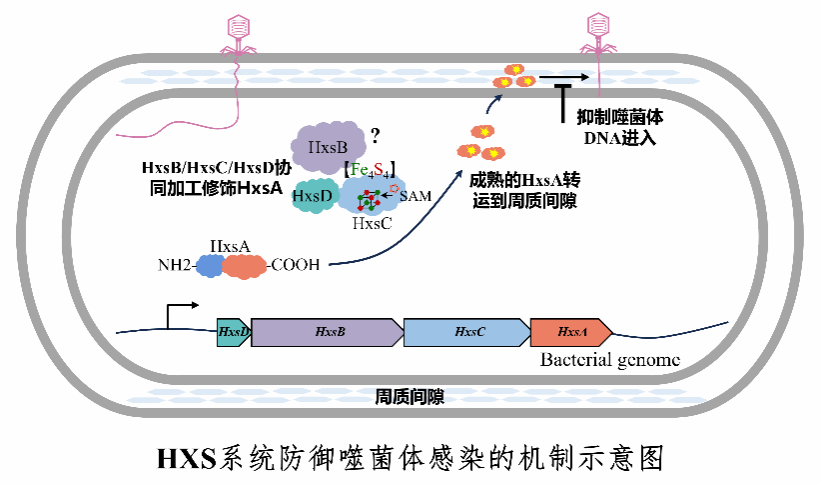
该研究发现了首个靶向噬菌体基因组注入这一最早期环节的细菌内源性防御系统,提出了细菌周质门控防御噬菌体感染的新范式。该发现不仅丰富了细菌抗噬菌体防御系统的理论体系,也为设计能够突破“入口拦截”屏障的高效噬菌体产品提供了理论指导。
五楼自拍
博士后李梦玲、已毕业博士生孙二超为论文共同第一作者,陶攀教授为论文通讯作者。该研究得到生猪数智育种与疫病防控学科突破先导项目、中央高校基础科研基金、国家自然科学基金、学院筑峰计划等项目支持。
审核人:陶攀
原文链接://www.nature.com/articles/s41467-026-70567-0

